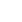
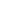La corrosion de la valve est l'une des principales causes de défaillance de la valve, la corrosion peut être divisée en six types, à savoir la corrosion électrique, la corrosion à haute température, la corrosion des crevasses, la corrosion piquante, la corrosion intergranulaire et la corrosion par friction. Pendant la corrosion, des réactions chimiques ou électrochimiques ont lieu à l'interface du métal, entraînant la transition du métal à un état oxydant (ionique). Cela réduira considérablement la résistance, la plasticité, la ténacité et d'autres propriétés mécaniques des matériaux métalliques, détruisent la géométrie des composants métalliques, augmentent l'usure entre les pièces, la détérioration des propriétés physiques électriques et optiques, raccourcissent la durée de vie de l'équipement, même provoqué des incendies, des explosions et d'autres accidents catastrophiques. Par conséquent, il est nécessaire d'empêcher la corrosion des métaux. Ci-dessous, nous vous présenterons 6 types de corrosion de la valve.
1. Corrosion électrique
Lorsque deux métaux différents sont en contact avec et exposés à des liquides et des électrolytes corrosifs, le courant galvanique fait corroder l'augmentation du courant. La corrosion est généralement localisée près du point de contact. La réduction de la corrosion peut être obtenue en électroplaçant les métaux différents.
2. Corrosion à haute température
Pour prédire l'effet de l'oxydation à haute température, nous devons tester les données: 1) la composition des métaux, 2) la composition de l'atmosphère, 3) la température et 4) le temps d'exposition. Il est bien connu, cependant, que la plupart des métaux légers (ceux qui sont plus légers que leurs oxydes) forment une couche d'oxyde non protégée qui se glisse au fil du temps. Il existe d'autres formes de corrosion à haute température, y compris la vulcanisation, la carburation, etc.
3. Corrosion des crevasses
Cela se produit dans les crevasses, qui bloquent la diffusion de l'oxygène, créant des régions d'oxygène élevé et faible qui varient en concentration en solution. En particulier, il peut y avoir des lacunes étroites dans les défauts des connecteurs ou des joints soudés, qui sont suffisamment larges (généralement 0,025 ~ 0,1 mm) pour permettre à la solution d'électrolyte d'entrer et de former une cellule galvanique court-circuit entre le métal dans les joints et le métal à l'extérieur des articulations et une forte corrosion locale se produit dans la fissure.
4. Piqûre
Lorsque le film de protection est détruit ou que la couche de produit de corrosion est décomposée, la corrosion locale ou les piqûres se produit. La rupture de la membrane forme une anode et un produit de membrane ou de corrosion inversé agit comme une cathode, établissant pratiquement un circuit fermé. Certains aciers inoxydables sont susceptibles de se promener en présence d'ions chlorure. La corrosion se produit à la surface d'un métal ou à un emplacement rugueux, en raison de cette inhomogénéité.

5. Corrosion intergranulaire
Il existe de nombreuses raisons de corrosion intergranulaire. Le résultat est une défaillance des mêmes propriétés mécaniques presque le long de la limite du grain du métal. La corrosion intergranulaire de l'acier inoxydable austénitique à des températures de 800-1500 F sans traitement thermique ou la sensibilisation au contact approprié est soumis à de nombreux agents corrosifs (427-816 ° C). Cette condition peut être éliminée par pré-recueil et éteinte à 2000 F (1093 ° C), en utilisant de l'acier inoxydable à faible teneur en carbone (C-0,03 max) ou du niobium ou du titane stabilisé.
6. Corrosion de Frition
D'après les forces physiques de l'usure et de la fracture, les métaux sont dissous par corrosion protectrice. L'effet dépend en grande partie de la force et de la vitesse. Des vibrations excessives ou une flexion métallique peuvent avoir des résultats similaires. La cavitation est une forme courante de pompe à corrosion, de fissuration de corrosion de contrainte, de stress à haute traction et d'une atmosphère corrosive provoquera une corrosion des métaux. Sous charge statique, la contrainte de traction de la surface du métal dépasse le point d'écoulement du métal et la corrosion se produit dans la zone où la contrainte est concentrée. Dans la corrosion alternée en métal et l'établissement d'une concentration à forte contrainte de pièces et de composants, éviter une telle corrosion peut être obtenue par un recuit précoce de soulagement de la contrainte ou la sélection de matériaux en alliage et d'options de conception appropriés. Fatigue de la corrosion. Nous associons généralement le stress statique à la corrosion.
Le stress peut entraîner des fissures de corrosion et la charge cyclique peut entraîner une corrosion de fatigue. La corrosion de la fatigue se produit lorsque la limite de fatigue est dépassée dans des conditions non corrosives. Étonnamment, lorsque les deux types de corrosion sont présents en même temps, les dommages sont encore plus importants. C'est pourquoi nous utilisons la meilleure protection contre la corrosion sous le stress alterné.
La corrosion désactivera la valve et affectera l'ensemble du projet. Il est donc nécessaire de l'embaumement. Ci-dessous, nous introduirons 4 mesures anti-corrosion de la vanne.
1. Sélection raisonnable des matériaux, toutes sortes de supports corrosifs sur différents matériaux ne sont pas les mêmes, il peut donc répondre aux exigences de performance sous la prémisse de la sélection des matériaux de médias corrosifs correspondants pour fabriquer des pièces de machine, en travaillant dans cet environnement moyen.
2. Protection de surface, après un certain traitement afin que la surface du matériau métallique ou ses produits forment une couche protectrice pour empêcher le métal et le milieu.
3. Traitement moyen, essayez de changer la nature du milieu corrosif, afin d'éviter ou de réduire la corrosion des métaux. Le traitement des médias est divisé en deux catégories: l'une consiste à supprimer ou à réduire les éléments nocifs dans les médias, tels que la déshumidification, la désoxydation, le dessalement, etc. L'autre consiste à ajouter des inhibiteurs de la corrosion.
4. Protection électrochimique, en utilisant la protection cathodique ou la méthode de protection anodique pour contrôler le métal dans l'électrolyte de la corrosion ou réduire la corrosion.
Temps de poste: juillet-28-2021